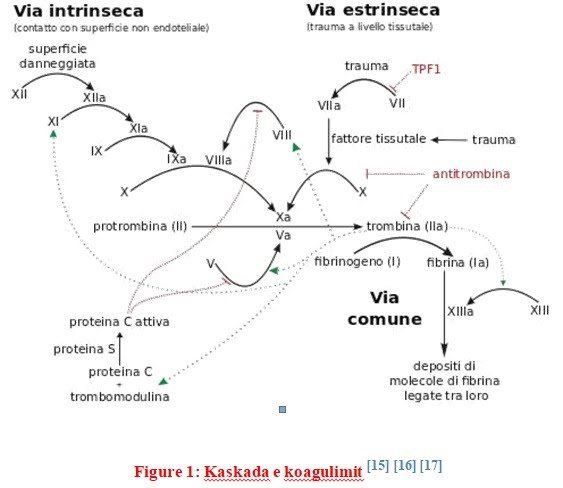
Pacientët mund të pësojnë tromboemboli polmonare, dr. Blendi Toska: Rëndësia e antikoagulimit në trajtimin e COVID-19

Share This Article
Dr. Blendi Toska përmes një studimi të realizuar mbi trajtimin e pacientëve me COVID-19 shpjegon dhe rëndësinë e Heparinës në trajtimin e pacientëve të infektuar që janë në terapi intensive.
Në këtë studim dr. Toska tregon veprimin e saj si antikoagulant duke shërbyer për të ndaluar formimin e trombeve apo procesin e trombozës vaskulare.
Statusi i hiperkoagulimit në pacientët kritikë COVID-19 duhet të monitorohet nga afër, dhe terapia antikoaguluese mund të konsiderohet në pacientët e zgjedhur. Terapia me antikoagulant parenteral LMWH mbetet si një zgjedhje trajtimi për pacientet në terapi intensive si një formë preventive e koagulimit intravaskular e diseminuar (DIC).
Studimet e fundit kanë treguar një risk që keta paciente mund të pësojne TEP(tromboembolia polmonare). Korelohen të dhena statistikore se një ndër komplikancat më të shpeshta te keta pacientë është tromboembolia polmonare. Rëndësia e trajtimit me LMWH vlen të theksohet se ofron një siguri në trajtimin në terapi intensive në rastet e komplikuara të pacientëve me COVID-19.
Përvec TEP është vërejtur se pacientët me COVID 19 shfaqin komplikacione si TVP(trombozë venoze profonde), disekacion te aortës. Prandaj LMWH mbetet një zgjedhje primare në trajtimin e pacientëve te prekur me COVID-19 në terapi intensive. Më shumë të dhëna klinike janë të nevojshme për të hetuar rolin e antikoagulimit në trajtimin COVID-19.
STUDIMI I PLOTE
ROLI I HEPARINES PARENTERALE (LMWH) NE TRAJTIMIN E PACIENTEVE TE INFEKUAR ME COVID-19 NE TERAPI INTENSIVE.
SARS-CoV-2 COVID-19 është përhapur në të gjithë botën. Sëmundja e shkaktuar nga SARS-CoV-2 COVID-19 është përhapur në të gjithë botën. Gati 20% e pacientëve janë në gjendje të rëndë ose kritike. SARS-CoV-2 shfrytëzon ACE-2(Angiotensin Converting Enzyme 2) për futjen në qelizat të ashtuquajtura “pritëse”. ACE2 luan një rol thelbësor në sistemin renin-angiotensin-aldosterone (RAAS), e cila ndodhet tek qelizat pneumocitare tipi II, rregullon presionin e gjakut dhe ekuilibrin e lëngjeve. ACE-2 gjithashtu mbron organet nga dëmtimet inflamatore dhe rregullon funksionin e zorrëve. ACE-2 mund të zberthehet nga dy proteaza, ADAM17 dhe TMPRSS2. ACE-
- e shpërbërë nga TMPRSS2 lejon hyrjen e qelizave SARS-CoV-2, ndërsa ACE-2 i zbërthyer ADAM17 ofron mbrojtje për organet. Mosfunksionimi ACE-2 i shkaktuar nga infeksioni SARS-CoV-2 përkeqëson COVID-19 dhe mund të inicojë dështim shumë-organesh (MOFS). [1] [2] [3] [4]
Pacientët kanë rezultate të ndryshme klinike, por ata me sëmundje paraprake kardiovaskulare (CV), hipertension, dhe kushte të tilla, pësojnë shënja klinike në mënyrë disproporcionale më të keqe. Infektiviteti i lartë i virusit SARS-CoV-2 është pjesërisht i lidhur me mutacione të reja në fushën e lidhjes së receptorit dhe adaptimin e një vendi të ndarjes së proteinës S-spike. Ngarkesa e vazhdueshme virale në individët asimptomatikë dhe para-simptomatikë rrit transmetimin e saj në komunitet. Virusi përdor receptorin ACE-2 për penetrim, të ndihmuar nga proteaza TMPRSS2. Lokalizimi i indeve të receptorëve që lidhet me COVDI-19 paraqesin simptoma dhe mosfunksionim të organeve. Rregullimi ACE-2 i shkaktuar nga virusi mund të zvogëlojë funksionin e tij, të zvogëlojë rolin e tij anti-inflamator dhe efekte të rritjes të angiotensinës II në pacientët e predispozuar. Limfopenia shfaqet herët dhe është prognostike, e lidhur potencialisht me uljen e CD4 + dhe disa qelizave CD8 + T. Kjo çon në çekuilibrim të përgjigjes imune të lindur
- të fituar, pastrim të vonuar viral si dhe makrofage dhe neutrofile të hiperstimuluara. Aktivizimi i rrugës së duhur të interferonit të tipit të duhur është kritik për dobësimin e virusit dhe reagimin e ekuilibruar të ekuilibruar. Aktivizimi i vazhdueshëm i imunitetit te pacientët e predispozuar, siç janë të moshuarit dhe ata me rrezik CV, mund të çojë në sindromën e hemofagocitozës, me amplifikim të pakontrolluar të prodhimit të citokinave, duke çuar në dështim shumë-organesh (MOFS) dhe vdekje. Përveç rrugëve të frymëmarrjes dhe mushkërive, sistemi kardiovaskular shpesh është i përfshirë herët në COVID-19, duke reflektuar në lëshimin e peptideve shumë të ndjeshme të troponinës dhe natriuretikut (NP), të cilat janë të gjitha jashtëzakonisht prognostike, veçanërisht në ato që tregojnë ngritje të vazhdueshme, së bashku me citokinat (IL-1; IL-6; TNF-α). Inflamacioni në sistemin vaskular mund të rezultojë në mikroangiopati difuze me trombozë. Inflamacioni në miokard mund të rezultojë në miokardit, dështim të zemrës, aritmi kardiake, sindromë akute koronare, përkeqësim të shpejtë dhe vdekje të papritur. Trajtimi i duhur për dështimin e zemrës, aritmitë, sindromën akute koronare dhe trombozat mbeten të rëndësishme. Strategjitë specifike të trajtimit të bazuar në prova për COVID-19 do të shfaqen me bashkëpunimin
| / [9] [10] [11] [12] [13] |
| [5] [6] [7] [8] |
e vazhdueshëm global për qasjet e shumta që vlerësohen, nder keto trajtimi me Heparine me peshe te vogel molekulare LMWH.
Zhvillimi i sindromës COVID-19 te pacientët me antikoagulant oral, dhe veçanërisht pranimi i tyre në njësitë e kujdesit intensiv me sindromë të rëndë akute të frymëmarrjes (SARS-CoV-2), i ekspozon ata në probleme specifike që lidhen me terapinë e tyre, përveç atyre që shoqërojnë infeksion viral akut. Pacientët me trajtim (vitamin -k- dipendent) të shtruar në spital me SARS-CoV-2 tregojnë paqëndrueshmëri të lartë të PT dhe INR për shkak të ndryshueshmërisë së metabolizmit të vitaminës K, dietë, agjërime, bashkë-medikamente, dëmtim të mëlçisë dhe dështim të zemrës. Pacientët në DOAC (direct oral anticoagulant) janë të ekspozuar ndaj trajtimit të shkaktuar nga ndërhyrje të konsiderueshme farmakologjike. Duke marrë parasysh karakteristikat farmakologjike të barnave antikoagulant oral, ndërveprimet e shumta farmakologjike për shkak të trajtimit të sëmundjes akute dhe domosdoshmërisë së mundshme të ventilimit mekanik me shtrimin në spital në njësitë e kujdesit intensiv, sugjerohet të zëvendësohet terapitë antikoaguluese orale (VKA dhe DOAC) me heparinë parenterale për të shmangur rrezikun
e trajtimit.
SARS-CoV-2 shpërndahet nëpërmjet bulzave (spërklave) në sistemin resipirator dhe futet në mushkëri nëpërmjet rrugëve te frymëmarrjes dhe pozicjonohet duke u ndihmuar nga ACE-2 (TMPRSS-2) në qelizat pneumocite tipi II, duke zbrazur materialin gjenetik (RNA) dhe qelizat bartëse bën translatimin e materialit gjenetik në Ribozome dhe nëpërmjet Proteazës transformohet në proteina virale nga ku paketohen dhe bëhen gati të dalin jashte citoplazmës së qelizës nëpërmjet ekzocitozës dhe më të shumta në numer gati për të infektuar të tjera qeliza pneumocite tipit II. [14] Duke u futur në nivel alveolar sistemi imun sic e shpjeguam aktivizohet duke aktivizuar neutrofilet dhe macrofagët ku depërtojne në alveol nëpërmjet gjakut kapilar dhe aktivizojnë clirimin e interleukinave (citokinave) IL-1; IL-6; TNF-α, të cilat janë përgjegjëse për rritjen e permeabilitetit, si dhe vazodilatim, nga ku rritja e permeabilitetit bën të mundur daljen e likidit në hapësiren peri-alveolare duke shkaktuar edemë alveolare dhe rrjedhimisht rritje të frekuencës resipratore (RR) duke shfaqur klinikisht Dispne (vështirësi në frymëmarrje), dhe në nivel kapilar ulje të PO2 për shkak të mos oksigjenimit si pasojë e dëmtimit të alveolave duke cuar ne hipoksiemi. Gjithashtu vërehet ndryshime presionesh ku kemi rritje të presionit hidrostatik dhe ulje të presionit kolloido-ozmotik. Neutrofilet bashkëveprojnë me alveolat (për të penetruar) nëpërmjet molekulave adezive të tipit ICAM-1 dhe ICAM-2, gjithashtu trupat Weibel-Palade përmbajne molekula adeziva të cilat nxiten nga mediatorë kimike (kemioceptorët), keto molekula adezive janë E-selectina dhe P-selectina të cilat janë të parat që aktivizohen. Neutrofilet tashmë janë gati të kalojnë nga kompartimenti intra-vaskular në atë extra-vaskular nëpërmjet kemiotazës duke bërë të mundur clirimin e komponentëve që jane IL-1; IL-6; TNF-α. Këto citokina janë regullatorë që rregullojnë amplifikimin e inflamacionit si dhe kohëzgjatja e tij. Të 3 keta elemente përbëjnë të ashtuquajturën “triada inflamatore”. IL-1 është nje citokinë pro-inflamatore që aktivizuon kemokinat, faktorin e rritjes (TNF); prostaglandina të cilat kanë një efekt vazodilatator e e cila në nivel sistemik të sistemit CV, ul presionin arterioz, ul frekuencen kardiake, ul volumin e gjakut të pompuar, ul
perfuzionin duke cuar ne hipoksiemi deri në MOFS (multi organ failure system); oksidi nitrik dhe veprojnë në hepar sëbashku me IL-6 duke alternuar proceset transaminacione. IL-6 së bashku me IL-1 veprojnë në nivel të Hipotalamit ku qelizat e endotelit përcaktojne praninë e tyre dhe prodhojne PGE2, prostaglandina e tipit E2 e cila sintetizon një mediator kimik që quhet “Adenilat ciklaza” i cili bën të mundur trasformimin e ATP ne AMP ciklike dhe keto të fundit nxitin qelizat neuronale që quhen “Warm” dhe keto nxitin rritjen e temperaturës, një ndër simptomat klinike kryesore te COVID-19. Kjo citokinë (IL-1) vepron në nivel kockor duke stimuluar riasorbim kockor, por njëkohësisht nxit katabolizmin proteinik në muskuj duke cliruar nxehtësi. Ne këtë rast tek pacientët simptomatikë vërehet një lodhje; dhimbje trupi difuze si dhe djegie dhe dhimbje të muskujve(mialgji). Kjo citokinë (IL-1) luan një rol të rëndësishëm pro-koagulant. Efekti pro-koagulant i IL-1 vërehet duke ndaluar sintezën e Proteinës C dhe Trombomodulinës. Proteina C është një glikoproteinë, Vitamina K-dipendente e cila caktivizohet nga IL-1 nga forma e saj aktive (APC) active protein C. Proteina C aktivizohet nga trombina së bashku me trombomodulinën e cila pëson nje ndryshim rrënjësor e cila nuk është më në gjëndje të kryejë rolin e saj si pro-koagulant, në këtë rast IL-1 ndalon aktivizimin e PC dhe trombomodulinës duke rritur efektin pro-koagulant pra nxit sintezën e “frenusit të proteinës C”. Trombina në bashkëveprim me trombomodulinën nga një pro-koagulant potent, kthehet në antikoagulan, por kur IL-1 ndalon trombomodulinën rritet efekti i Trombinës si pro-koagulant. Proteina C caktivizon faktorin V(faktori Leiden) si dhe faktorin VIII, të rëndësishëm në procesin e koagulimit, pra ngadalësojnë formimin e koagulit, njsoj si fenat e një makine për të ulur shpejtësinë., gjithashtu Proteina C nxit fibrinolizën nëpërmjet tissutal-Activating-Plasminogen (t-PA) duke frenuar ndaluesin e saj PAI(plasminogen-activator-inhibitor). Për këtë arsye një ndër komplikancat e pacientëve të infektuar me COVID-19 është Trombo-Embolia, gjithashtu trombozë mikrovaskulare duke shkaktuar Iskemi dhe MOFS (Multi Organ Failure System).
Heparina me peshë te vogël molekulare (LMWH) dhe veprimi i saj si antikoagulant shërben për të ndaluar formimin e trombeve apo procesin e trombozës vaskulare(mikro). LMWH frenon procesin e koagulimit duke u lidhur në AT(antitrombina) përmes një sekuence pentasakaride. Kjo lidhje çon në një ndryshim konformues të AT i cili përshpejton frenimin e tij të faktorit të aktivizuar X (faktori Xa). Pasi të ndahet, LMWH është e lirë të lidhet me një molekulë tjetër antitrombine dhe më pas frenon faktorin Xa të aktivizuar. Në dallim nga AT i aktivizuar me heparin, AT i aktivizuar me LMWH nuk mund të frenojë trombinën (faktori IIa), por mund të frenojë vetëm faktorin e koagulimit Xa. [18]
Duke marrë parasysh karakteristikat klinike dhe koaguluese të sëmundjes kritike të koronavirus 2019 (COVID-19) të pacientëve me akro-ishemi në njësinë e kujdesit intensiv (ICU).
Një studim retrospektiv përfshiu 7 pacientë kritikë COVID-19 me akro-ishemi në një qendër të vetme në Wuhan, nga 4 shkurt deri më 15 shkurt 2020. Të dhënat klinike dhe laboratorike para dhe gjatë qëndrimit të ICU u analizuan.
Mosha mesatare prej 7 pacientësh ishte 59 vjeç dhe 4 prej tyre ishin burra. 3 prej tyre ishin të lidhur me komorbiditete themelore. Ethe, kollë, dispne dhe diarreja ishin simptoma klinike të zakonshme. Të gjithë pacientët kishin prezantime akro-iskemie përfshirë cianozën e gishtit / shputës, demtim te lëkurës dhe gangrenën e thatë. D-dimer, fibrinogjen dhe produkt i degradimit i fibrinogjenit (FDP) u ngritën në mënyrë të konsiderueshme në shumicën e pacientëve. Koha e protrombinës (PT) ishte zgjatur në 4 pacientë. Nivelet e D-dimerit dhe FDP u rritën në mënyrë progresive kur COVID-2019 u përkeqësuan, dhe 4 pacientë u diagnostikuan me koagulim të përhapur intravaskular të shpërndarë (DIC). 6 pacientë morën trajtim me heparinë me peshë të ulët molekulare (LMWH), pas së cilës D-dimer dhe FDP i tyre ranë, por nuk pati ndonjë përmirësim të ndjeshëm në simptomat klinike. 5 pacientë vdiqën më në fund dhe koha mesatare nga akro-ishemi deri në vdekje ishte 12 ditë. [19]
Statusi i hiperkoagulimit në pacientët kritikë COVID-2019 duhet të monitorohet nga afër, dhe terapia antikoaguluese mund të konsiderohet në pacientët e zgjedhur. Terapia me antikoagulant parenteral LMWH mbetet si një zgjedhje trajtimi për pacientet në terapi intesnive si një formë preventive e koagulimit intravaskular e diseminuar (DIC). Studimet e fundit kanë treguar një risk që keta paciente mund të pësojne TEP(tromboembolia polmonare). Korelohen të dhena statistikore se një ndër komplikancat më frekuente te keta pacientë është tromboembolia polmonare. Rëndësia e trajtimit me LMWH vlen të theksohet se ofron një siguri në trajtimin në terapi intensive në rastet e komplikuara të pacintëve me COVID-19. Përvec TEP është vërejtur se pacientët me COVID 19 shfaqin komplikacjone si TVP(trombozë venoze profonde), disekacion te aortës. Prandaj LMWH mbetet një zgjedhje primare në trajtimin e pacientëve te prekur me COVID 19 në terapi intensive. Më shumë të dhëna klinike janë të nevojshme për të hetuar rolin e antikoagulimit në trajtimin COVID-2019.
REFERENCAT
- Viruses. 2020 Apr 28;12(5). pii: E491. doi: 10.3390/v12050491
- Department of Pharmacology, School of Life Dentistry at Tokyo, The Nippon Dental University, Tokyo 102-0071, Japan.
- Meikai University Research Institute of Odontology (M-RIO), Saitama 3500283, Japan.
- Faculty of Life Sciences, Prefectural University of Hiroshima, Hiroshima 7270023, Japan
- University of Ottawa Heart Institute and University of Ottawa, Ottawa, Ontario, Canada; Departments of Medicine and Cellular & Molecular Medicine, University of Ottawa, Canada.
- University of Ottawa Heart Institute and University of Ottawa, Ottawa, Ontario, Canada; Department of Anesthesiology, Critical Care and Burn Center, Lariboisière – Saint-Louis Hospitals, DMU Parabol, AP-HP Nord, University of Paris, France; Inserm UMR-S 942, Cardiovascular Markers in Stress Conditions (MASCOT), University of Paris, Paris, France.
- Department of Cardiology, Renmin Hospital of Wuhan University, Wuhan, China; Medical Science Research Center, Zhongnan Hospital of Wuhan University, Wuhan, China; Basic Medical School, Wuhan University, Wuhan, China
- Circulation. 2020 Apr 15. doi: 10.1161/CIRCULATIONAHA.120.047549.
- Haemostasis and Thrombosis Center, Cremona Hospital, Viale Concordia 1, 26100, Cremona, Italy. [email protected].
- Haemostasis and Thrombosis Center, Cremona Hospital, Viale Concordia 1, 26100, Cremona, Italy.
- Division of Internal Medicine, Cremona Hospital, Viale Concordia 1, 26100 Cremona, Italy.
- Division of Infectious Disease, Cremona Hospital, Viale Concordia 1, 26100 Cremona, Italy.
- Intern Emerg Med. 2020 Apr 15. doi: 10.1007/s11739-020-02331-1.
- 2020 Jun; 215: 108427.Published online 2020 Apr 20. doi: 10.1016/j.clim.2020.108427
- Pallister CJ, Watson MS (2010). Haematology. Scion Publishing. pp. 336–347. ISBN 978-1-904842-39-2.
- “COAGULATION FACTOR”. Clotbase.bicnirrh.res.in. Retrieved 20 May 2018.
- Hoffbrand, A. V. (2002). Essential haematology. Oxford: Blackwell Science. pp. 241–243. ISBN 978-0-632-
- Jeske W, Walenga J, Fareed J. Differentiating between the Low-Molecular-Weight-Heparin used for VTE treatment and prophylaxis. Thromb Clin. 2008;2(3)
- Zhonghua Xue Ye Xue Za Zhi. 2020 Mar 28;41(0):E006. doi: 10.3760/cma.j.issn.0253-2727.2020.0006.